胃病引发的饥饿感,本质是胃黏膜损伤与胃酸分泌失衡的“双重陷阱”。当胃黏膜受损时,身体会启动修复机制,加速能量代谢以促进细胞再生,这种“修复性饥饿”会通过神经信号传递至大脑,引发持续的饥饿感。例如,胃溃疡患者因胃黏膜深层损伤,修复过程需消耗大量蛋白质与能量,导致患者即使刚进食仍感饥饿。
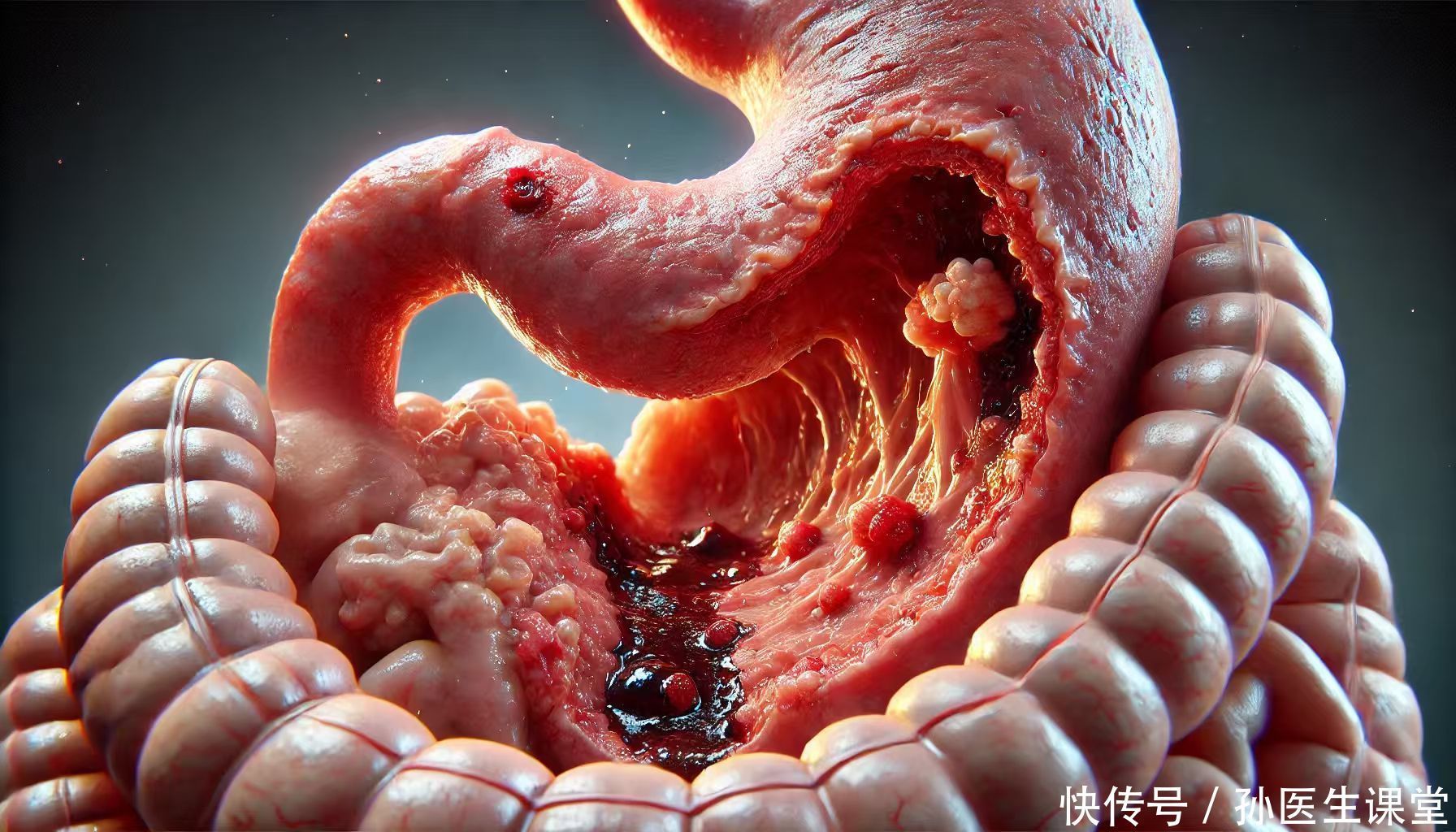
更隐蔽的是胃酸分泌异常。胃食管反流病患者常因胃酸反流刺激食管,引发“假性饥饿”——大脑误将食管灼烧感解读为胃排空信号,导致患者频繁进食。研究表明,此类患者胃饥饿素(刺激食欲的激素)分泌量较常人高出30%,进一步加剧饥饿感。
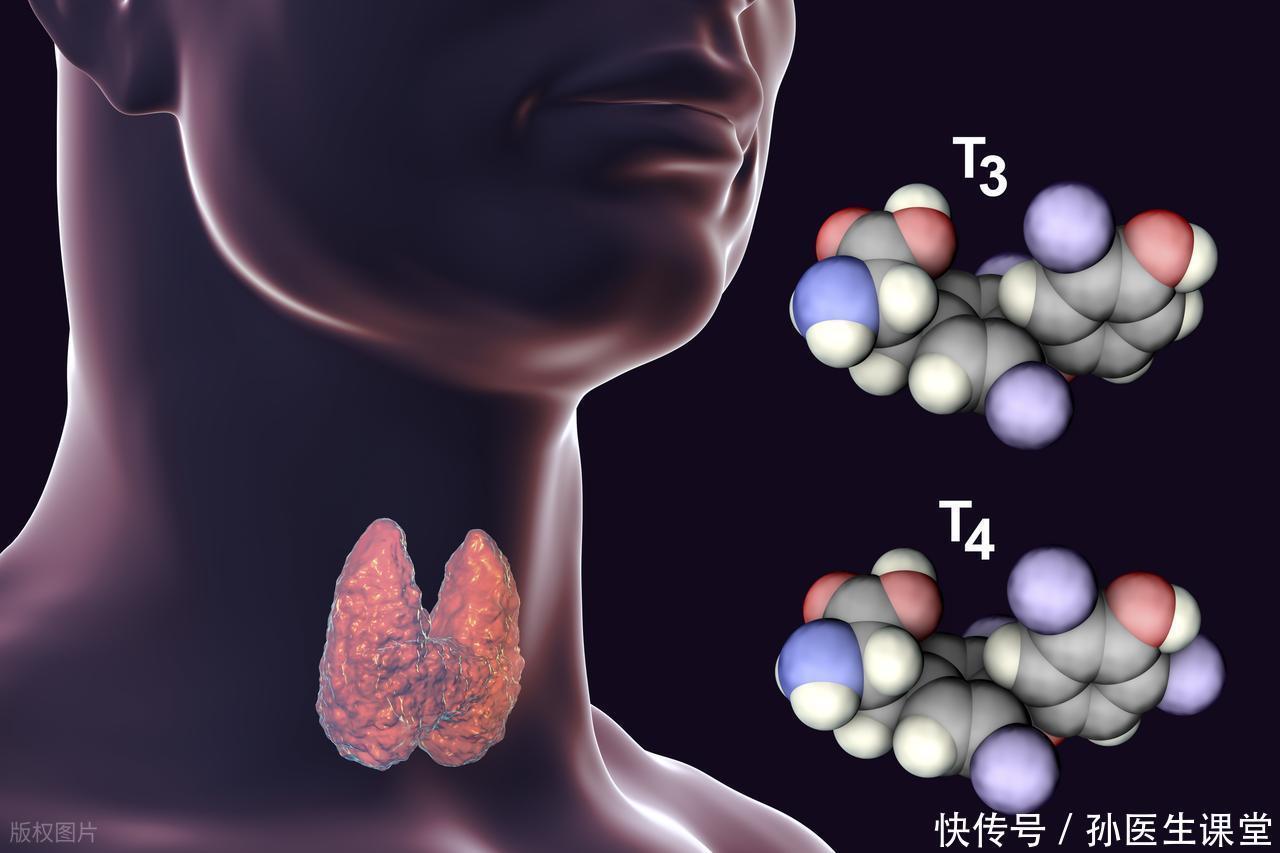
代谢失控:甲状腺与胰岛素的“拉锯战”甲状腺功能亢进症患者的饥饿感,源于甲状腺激素过量引发的“代谢风暴”。甲状腺激素会加速全身细胞代谢,使能量消耗速度提升2-3倍。患者即使每日摄入4000千卡热量,仍可能因能量缺口感到饥饿,同时伴随心悸、手抖等症状。
糖尿病患者的饥饿感则与胰岛素抵抗密切相关。当细胞对胰岛素敏感性下降时,血糖无法进入细胞供能,导致身体误判能量不足,持续刺激饥饿中枢。这种“细胞饥饿”会引发多食、多饮、多尿的“三多”症状,若未及时干预,可能发展为代谢综合征。
肝脏与心理:被忽视的“饥饿推手”脂肪肝患者的饥饿感,源于肝脏糖原储备能力的下降。肝脏是调节血糖的核心器官,当肝细胞脂肪浸润超过30%时,糖原合成与分解功能受损,导致血糖波动加剧。患者常在餐后2-3小时出现低血糖样饥饿,伴随乏力、注意力不集中。
心理因素对饥饿感的影响同样显著。长期压力会激活下丘脑-垂体-肾上腺轴,促使皮质醇分泌增加。皮质醇不仅会刺激食欲,还会降低瘦素(抑制食欲的激素)敏感性,形成“压力-饥饿-暴食”的恶性循环。一项针对职场人群的研究显示,持续高压状态下,个体每日热量摄入平均增加15%。
行动建议:从“被动应对”到“主动管理”建立饮食日志:记录每日进食时间、食物种类及饥饿感出现节点,识别饮食模式与症状的关联性。优化饮食结构:增加膳食纤维(如燕麦、西兰花)与优质蛋白(如鸡蛋、鱼类)摄入,延长饱腹感持续时间。定期医学筛查:若伴随体重下降、心悸、多汗等症状,需检测甲状腺功能、空腹血糖及糖化血红蛋白。 管理心理压力:通过正念饮食训练、规律运动等方式调节皮质醇水平,打破情绪化进食循环。
管理心理压力:通过正念饮食训练、规律运动等方式调节皮质醇水平,打破情绪化进食循环。异常饥饿感是身体发出的“求救信号”,其背后可能隐藏着从胃黏膜损伤到代谢失衡的复杂病理。通过科学饮食管理、定期医学筛查与心理调节,我们不仅能缓解症状,更能从源头预防疾病进展。记住,真正的健康管理最安全的线上配资平台,始于对每一个细微身体信号的重视。
元鼎证券官网-极速开户,专业团队全程服务!提示:本文来自互联网,不代表本网站观点。